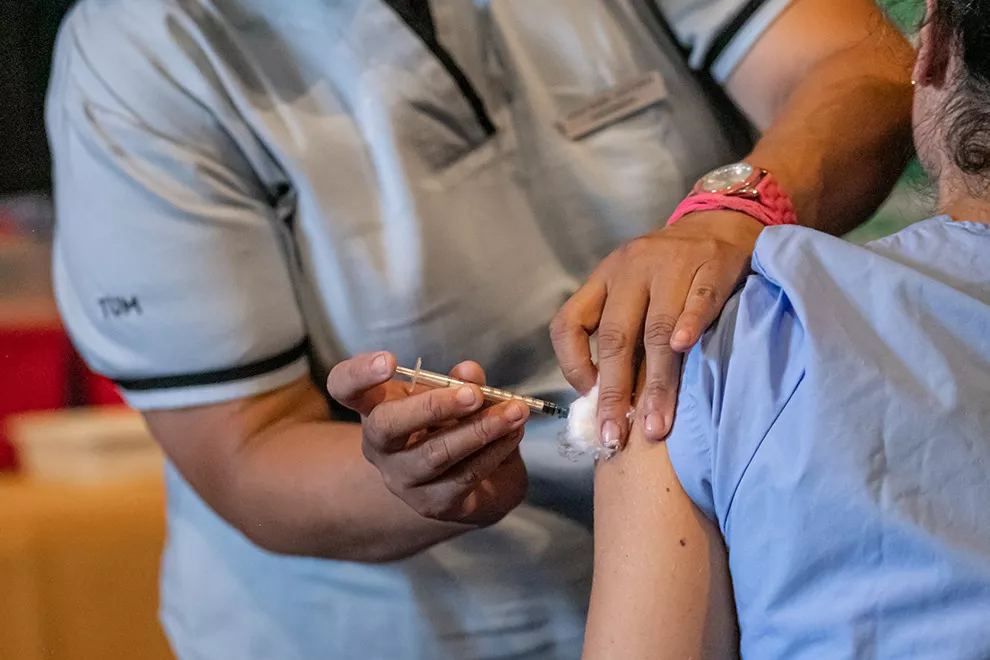
Se reitera que la vacunación antigripal continúa siendo la principal herramienta de prevención.
Este antiviral puede convertirse en el primer y único fármaco oral indicado para fases iniciales de la enfermedad.
Salud05 de noviembre de 2021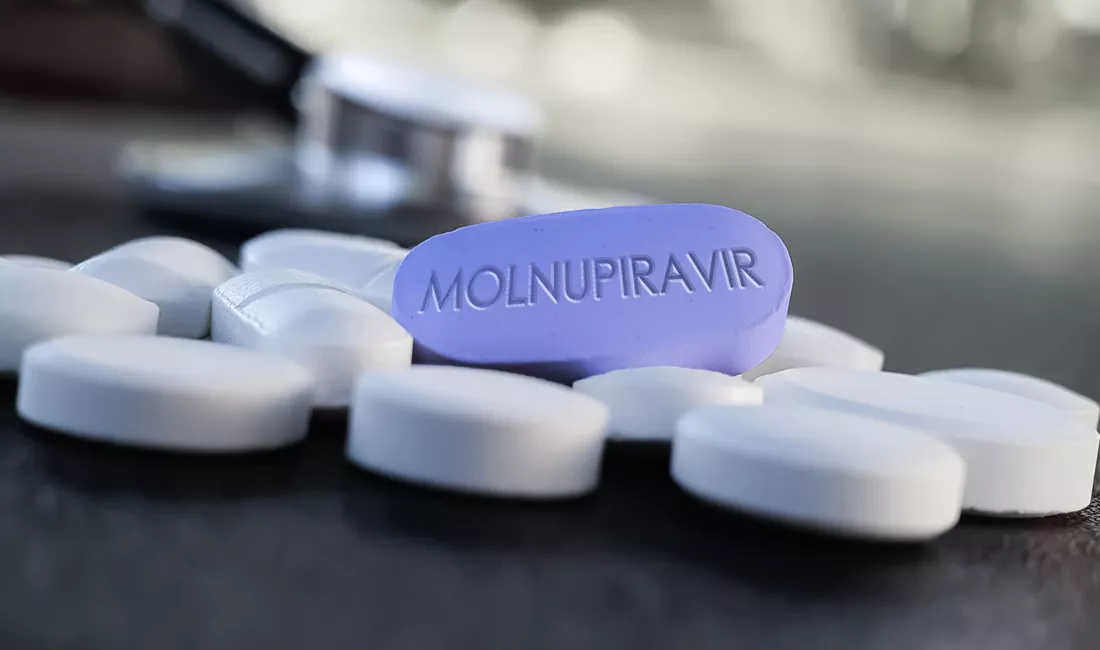
La farmacéutica estadounidense Merck anunció el pasado miércoles un acuerdo que podría permitir que las versiones genéricas de su fármaco contra el Covid-19 para las personas infectadas por la enfermedad estén ampliamente disponibles en los países pobres cuando las agencias reguladoras le den luz verde.
Merck ha rubricado con el Banco de Patentes de Medicamentos (MPP) un acuerdo de licencia voluntaria para facilitar el acceso mundial asequible al molnupiravir. Sujeto a la aprobación reglamentaria, el acuerdo ayudará a proporcionar un amplio acceso en 105 países de ingresos bajos y medios. El Reino Unido anunció este jueves que es el primer país del mundo en autorizar el molnupiravir. Los organismos reguladores de medicamentos de Estados Unidos y la Unión Europea, FDA y EMA, ya han iniciado una evaluación del fármaco. Ésta última dio luz verde ayer a los estados miembros para que lo utilicen bajo la vía de emergencia.
¿Por qué es importante facilitar el acceso a este antiviral?
Esto es una respuesta a la expectación que el antiviral que puede convertirse en el primer y único fármaco oral indicado para fases iniciales del Covid-19. Acerca la posibilidad de tratar a los pacientes de forma ambulatoria y evitar que progresen a fases más graves. El pasado 1 de octubre las compañías americanas MSD y Ridgeback Biotherapeutics anunciaron en una nota de prensa que su antiviral había reducido un 50% el riesgo de hospitalización o muerte en pacientes adultos no hospitalizados con Covid-19 de leve a moderada y al menos un factor de riesgo de progresar a enfermedad grave.
Los resultados proceden de un análisis interino del ensayo de fase III Move-Out, que mostraron que, a los 29 días desde la aleatorización, el 14,1% de los pacientes tratados con placebo (53/377) fueron hospitalizados o fallecieron, en comparación con un 7,3% de hospitalizaciones entre los pacientes que recibieron molnupiravir (28/385), ya que no se reportaron muertes en el grupo del antiviral y sí ocho en el del placebo.
El ensayo se llevó a cabo en pacientes no vacunados, que habían comenzado a experimentar síntomas en los 5 días previos al inicio del tratamiento. Todos presentaban algún factor de riesgo, como tener más de 60 años, obesidad, diabetes o enfermedad cardiaca, entre otros. En un 40% de los pacientes incluidos en el análisis había datos de secuenciación viral, que demostraron que el fármaco fue eficaz frente a las variantes Gamma, Delta y Mu, y su perfil de seguridad fue comparable al placebo.
Desde MSD España, su director médico, Joaquín Mateos, califica los resultados de "muy relevantes". Explica que, de ser aprobado, el tratamiento se tomaría durante cinco días, dos veces al día, y que es importante comenzar el antiviral en los cinco primeros días desde que empezaron los síntomas. "En esta ventana de tiempo suele tratarse de pacientes que acuden a Atención Primaria en busca de un diagnóstico para su cuadro de síntomas".
La EMA y la FDA ya han iniciado la revisión continua de la información disponible sobre el compuesto para la autorización de uso de emergencia. El regulador norteamericano ha convocado una reunión el próximo 30 de noviembre con su comité asesor para ayudarle a adoptar una decisión sobre la aprobación del medicamento y en qué condiciones podría ser usado. "Existe una necesidad de disponer de fármacos antivirales eficaces para el tratamiento del Covid-19", advierte Antonio Vallano, coordinador del Programa de Armonización Farmacoterapéutica del Servicio Catalán de Salud y portavoz de la Sociedad Española de Farmacología Clínica (SEFC).
De momento el único antiviral autorizado en el tratamiento del Covid-19 es remdesivir, "cuyos resultados han sido motivo de un gran debate y discusión sobre la relevancia clínica de su eficacia. Además, otros antivirales que inicialmente fueron utilizados, como lopinavir/ritonavir, posteriormente se demostró que no eran eficaces", resalta el farmacólogo.
La importancia del acceso: debe usarse en los cinco primeros días desde la infección
La eventual disponibilidad de molnupiravir cubriría una laguna en el abordaje del Covid-19, coincide José Ramón Arribas, jefe de Sección de Medicina Interna del Hospital La Paz (Madrid) y experto de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (Seimc). "Una de las necesidades no resueltas es disponer de un antiviral en los primeros días de la enfermedad, que es cuando la replicación viral es la causante de la mayor parte del daño. Para que funcione tiene que emplearse en los primeros días de la enfermedad, y esto tiene unas implicaciones globales: para muchos países debe tener un precio adecuado y, aunque así sea, si hay dificultad para acceder a los test diagnósticos, tampoco podrá ser útil", alerta.
La necesidad de ceñirse a este marco temporal de cinco días también "supone una limitación importante en un país como España", interpreta Jesús Sierra, jefe de Sección de Uso Racional de la Farmacia del Hospital de Jerez de la Frontera y portavoz de la Sociedad Española de Farmacia Hospitalaria (SEFH). Para Sierra, es muy probable que la confirmación de casos positivos de Covid-19 se esté demorando más allá de estos cinco días con síntomas, debido a la alta tasa de inmunización de la población, que ha reducido el miedo al Covid-19. Asimismo, porque la infección por SARS-CoV-2 puede confundirse con cuadros catarrales causados por otros patógenos respiratorios menos peligrosos.
El experto insiste en la importancia de conocer el detalle de los resultados del ensayo clínico de fase III para determinar si existe un beneficio individual del fármaco en subgrupos de población por factores de riesgo.
Pero para Arribas no tendría sentido un uso muy restringido en España: "Aunque es muy probable que la infección sea más leve en los pacientes vacunados, en el momento actual, ante un paciente positivo y con factores de riesgo, no tendría sentido hacer una distinción entre vacunados y no vacunados, porque hay una ventana de oportunidad en los primeros cinco días desde el inicio de síntomas y en los hospitales constatamos que hay pacientes con fracasos vacunales graves".
Algunas cuestiones sin resolver del antiviral
Otra incógnita es el potencial riesgo de desarrollo de resistencias. Desde MSD informan de que "la corta duración del tratamiento, de cinco días, otorga al virus pocas oportunidades de evolucionar hacia formas resistentes". En el Move-Out no dio signos de debilidad ante las variantes y según Sierra, es previsible que su eficacia se mantenga debido a su acción antiviral de amplio espectro. Por este motivo, "es un medicamento al que se podría recurrir en el caso de que surgiera alguna variante que comprometiera la protección de las vacunas", observa. "Molpunavir actúa como un sustrato competitivo de la ARN polimerasa dependiente del ARN codificado (RdRp) por el SARS-CoV-2, e induce un efecto antiviral a través de la acumulación de mutaciones con cada ciclo de replicación viral. Los estudios preclínicos revelan una actividad antiviral de amplio espectro contra los coronavirus, incluido el SARS-CoV-2, con una alta barrera a la resistencia", apunta Vallano.

Se reitera que la vacunación antigripal continúa siendo la principal herramienta de prevención.

Las instituciones sanitarias detectaron la presencia de la bacteria Listeria monocytogenes.

Te brindamos una mirada profunda sobre cómo ciertas conductas humorísticas pueden vincularse con emociones ocultas, necesidades internas y particularidades del funcionamiento mental.

Aumentaron un 17% los casos de hantavirus. La cartera sanitaria alertó sobre zonas de riesgo en cuatro regiones del país.
Se trata de una terapia para casos agresivos que implica editar la genética del paciente.
Un trabajo de científicos estadounidenses y austríacos pone en la mira el uso de influencers en las redes sociales.

El presidente de Estudiantes fue crítico del modelo actual y aseguró que la Liga Profesional debería estar entre las 5 mejores del mundo.

Esta calle estrecha sorprende por la convivencia entre el paso del tren, viviendas familiares y el auge de los cafés turísticos.

El dólar oficial subió de forma diaria, pero cierra la semana con un avance de solo $9 o 0,6%, lo que presupone que no influyó negativamente la ampliación de las bandas en enero.

Los colectivos partirán desde la Plaza de la Intendencia-Héroes de Malvinas a partir de las 17:00 horas.

La actividad deportiva en el inicio del fin de semana, disponible por internet y televisión.

Las fiestas de Navidad y Año Nuevo son momentos de unión, regalos y celebraciones, pero también generan una intensa cantidad de residuos.

Rayas, tejidos nobles, colores neutros y espíritu costero: la estética marítima vuelve renovada y se impone como una de las tendencias más fuertes del momento en redes sociales y street style.
Lo determinó el Ministerio de Salud Pública y Bienestar Social del país.

Se reitera que la vacunación antigripal continúa siendo la principal herramienta de prevención.

La morosidad de los préstamos a familias llegó al 7,8% en octubre de 2025 y triplicó el nivel interanual.